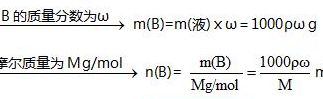摩尔分数公式
摩尔分数=(C/M)/[(100-C)/M+C/M]=CM/[100M-C(M-M)]混合物中溶质B的物质的量与混合物各组分物质的量之和的比值,称为摩尔分数。
摩尔分数计算公式是c=n/v,单位:mol/L。物质的量浓度就是单位体积内物质的摩尔数。摩尔简称摩,旧称克分子、克原子,符号为mol,是物质的量的单位,是国际单位制7个基本单位之一。每1摩尔任何物质(微观物质,如分子、原子等)含有阿伏加德罗常量(约02×10__)个微粒。
摩尔分数计算公式是xB=nB/n,混合物中溶质B的物质的量与混合物各组分物质的量之和的比值,称为摩尔分数,用符号xB表示,n为混合物的物质的量。摩尔分数影响因素只能是某物质的物质的量以及总的混合物的物质的量,温度、压力、状态等因素均不影响摩尔分数的大小。
需要知道溶质的分子量和溶剂的分子量才可以进行转换,转换方法按如下:设该物质的分子量为M1,质量分数为C%,溶剂的分子量为M2,溶液的质量为100。
摩尔分数的计算公式是什么?
1、摩尔分数=(C/M)/[(100-C)/M+C/M]=CM/[100M-C(M-M)]混合物中溶质B的物质的量与混合物各组分物质的量之和的比值,称为摩尔分数。
2、摩尔分数计算公式是c=n/v,单位:mol/L。物质的量浓度就是单位体积内物质的摩尔数。摩尔简称摩,旧称克分子、克原子,符号为mol,是物质的量的单位,是国际单位制7个基本单位之一。每1摩尔任何物质(微观物质,如分子、原子等)含有阿伏加德罗常量(约02×10__)个微粒。
3、摩尔分数计算公式是xB=nB/n,混合物中溶质B的物质的量与混合物各组分物质的量之和的比值,称为摩尔分数,用符号xB表示,n为混合物的物质的量。摩尔分数影响因素只能是某物质的物质的量以及总的混合物的物质的量,温度、压力、状态等因素均不影响摩尔分数的大小。
摩尔分数是怎么算出来的
摩尔分数=(C/M)/[(100-C)/M+C/M]=CM/[100M-C(M-M)]混合物中溶质B的物质的量与混合物各组分物质的量之和的比值,称为摩尔分数。
摩尔分数计算公式是c=n/v,单位:mol/L。物质的量浓度就是单位体积内物质的摩尔数。摩尔简称摩,旧称克分子、克原子,符号为mol,是物质的量的单位,是国际单位制7个基本单位之一。每1摩尔任何物质(微观物质,如分子、原子等)含有阿伏加德罗常量(约02×10__)个微粒。
摩尔分数计算公式是 混合物中溶质B的物质的量与混合物各组分物质的量之和的比值,称为摩尔分数,用符号xB表示,n为混合物的物质的量。摩尔分数影响因素只能是某物质的物质的量以及总的混合物的物质的量,温度、压力、状态等因素均不影响摩尔分数的大小。
混合物中溶质B的物质的量与混合物各组分物质的量之和的比值,称为摩尔分数(mole fraction),用符号xB表示。xB=nB/n 式中:xB表示溶质B的摩尔分数,单位为1;nB表示溶质B的物质的量,单位为mol;n为混合物的物质的量,单位为mol。显然,溶液中各组分摩尔分数之和等于1,即∑xi=1。
混合物或溶液中的一种物质的物质的量与各组分的物质的量之和之比,即为该组分的摩尔分数。可以指混合物中某一组分的物质的量与混合物物质的量之和之比。也可以指溶液中溶质的物质的量与溶质溶剂物质的量之和之比,经常用于气体混合物中某气体的物质的量与混和气体中各组分的物质的量之和之比。
摩尔分数计算公式是xB=nB/n,混合物中溶质B的物质的量与混合物各组分物质的量之和的比值,称为摩尔分数,用符号xB表示,n为混合物的物质的量。摩尔分数影响因素只能是某物质的物质的量以及总的混合物的物质的量,温度、压力、状态等因素均不影响摩尔分数的大小。
摩尔分数计算公式
1、摩尔分数=(C/M)/[(100-C)/M+C/M]=CM/[100M-C(M-M)]混合物中溶质B的物质的量与混合物各组分物质的量之和的比值,称为摩尔分数。
2、摩尔分数计算公式是c=n/v,单位:mol/L。物质的量浓度就是单位体积内物质的摩尔数。摩尔简称摩,旧称克分子、克原子,符号为mol,是物质的量的单位,是国际单位制7个基本单位之一。每1摩尔任何物质(微观物质,如分子、原子等)含有阿伏加德罗常量(约02×10__)个微粒。
3、摩尔分数计算公式是xB=nB/n,混合物中溶质B的物质的量与混合物各组分物质的量之和的比值,称为摩尔分数,用符号xB表示,n为混合物的物质的量。摩尔分数影响因素只能是某物质的物质的量以及总的混合物的物质的量,温度、压力、状态等因素均不影响摩尔分数的大小。
4、xB=nB/n 式中:xB表示溶质B的摩尔分数,单位为1;nB表示溶质B的物质的量,单位为mol;n为混合物的物质的量,单位为mol。显然,溶液中各组分摩尔分数之和等于1,即∑xi=1。摩尔分数是指混合物中物质B的溶质的量nB与混合物的总物质的量n之比,用符号xB表示,摩尔分数的SI单位为1,即没有单位。
5、混合物或溶液中的一种物质的物质的量与各组分的物质的量之和之比,即为该组分的摩尔分数。可以指混合物中某一组分的物质的量与混合物物质的量之和之比。也可以指溶液中溶质的物质的量与溶质溶剂物质的量之和之比,经常用于气体混合物中某气体的物质的量与混和气体中各组分的物质的量之和之比。
6、需要知道溶质的分子量和溶剂的分子量才可以进行转换,转换方法按如下:设该物质的分子量为M1,质量分数为C%,溶剂的分子量为M2,溶液的质量为100。
摩尔分数和体积分数的换算怎么算?
1、质量分数=体积分数*密度=摩尔分数*摩尔质量。体积分数=摩尔分数*24(标况下理想气体)。氧气的摩尔分数等于氧气的体积分数。所以氧气的摩尔分数是21%摩尔分数,是很不规范的说法,正确的说法是“物质的量分数”。质量分数=体积分数*密度=摩尔分数*摩尔质量体积分数=摩尔分数*24(标况下理想气体)。
2、质量分数=体积分数*密度=摩尔分数*摩尔质量体积分数=摩尔分数*24(标况下理想气体)。
3、P表示压强、V表示气体体积、n表示物质的量、T表示绝对温度、R表示气体常数,所有气体R值均相同。体积与摩尔数的关系:体积分数一般用于气体混合物,指某气体体积所占混合气体总体积的比例。摩尔分数则可用于气、体、液体等混合物,指某物质的物质的量占各组分的物质的之和量的比例。
4、那么氮气的气体体积分数是多少?百分之50。
5、推论5:同温同压同质量,体积与摩尔质量成反比 推论6:同温同体积同质量,压强与摩尔质量成反比 就是一个公式:PV=nRT(P压强 V体积 R常数 T温度),及其变式:PM=ρRT(P压强 ρ密度 R常数 T温度)的应用 运用的时候,注意审题,准确的找出相同的条件,然后把推论运用进去。
6、现在的题目中,百分含量一般可以理解为物质的量分数,即该组分的物质的量除以总物质的量得到的数值。例如合成氨反应达到平衡时,假设氮气、氢气、氨气的物质的量均为1摩尔,则氮气的物质的量分数为1/3。
摩尔比和摩尔分数的转化公式
摩尔分数为百分数,摩尔分率也即摩尔比,两者不同。
摩尔分率是指某一组分在全部组分中所占摩尔比,通常以y表示气相摩尔分率,以x表示液相庳尔分率。如果某混合气体中含有A、b两种组分,而a为可溶组分,用液相吸收剂c与此混合气体相接触。由于A为可溶组分,故将溶入C中。
若工业上生产质量分数为31%的盐酸(ρ=15g/cm3)2000kg,理论上需标准状况下的氯气的体积为多少?[小结](1)明确计算依据:参加反应物质的物质的量之比等于化学计量数之比;(2)在综合计算中应善于将其它物理量转化为物质的量来进行计算;(3)应注意物理量的规范化表示和计算过程的规范化。
等温低浓度吸收可以用摩尔比代替摩尔分数的原因是:溶质在气液两相中的摩尔分数均小于0.1时,吸收过程称为低浓度吸收。对低浓度系统,计算时可用摩尔分数代替摩尔比,用混合气体量代替惰性气体量,用溶液量代替溶剂量。
文章声明:以上内容(如有图片或视频亦包括在内)除非注明,否则均为网友提供或互联网,转载或复制请以超链接形式并注明出处。